隨著物聯網技術的飛速發展與廣泛應用,其觸角正深入現代農業的各個角落,一場深刻的產業變革正在醞釀。其中,將物聯網技術與農作物生產、管理相結合,并以此為基礎構建系統化、智能化的生物質能資源數據庫信息系統,已成為推動農業可持續發展和能源結構優化的重要前沿方向。這一融合不僅預示著農業生產模式的升級,更將為生物質能的科學開發與高效利用開辟全新路徑。
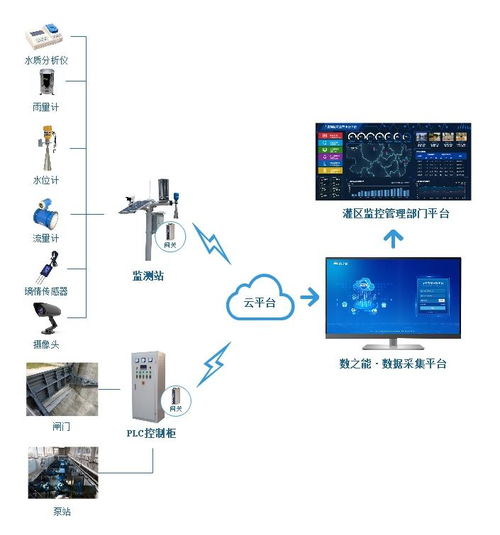
物聯網的核心在于通過傳感器、射頻識別、全球定位系統等信息傳感設備,按約定的協議,將任何物品與互聯網連接起來,進行信息交換和通信,以實現智能化識別、定位、跟蹤、監控和管理。當這項技術應用于廣闊的農田,每一株作物、每一塊土地都將成為網絡中的一個節點。土壤濕度傳感器實時監測墑情,環境傳感器收集光照、溫度、二氧化碳濃度數據,生長監測設備記錄作物的株高、葉面積等生物信息。這些海量、連續、精準的數據通過無線網絡匯聚到云端平臺,使得農作物生長過程首次得以被全面、動態地數字化呈現。
正是在此全面感知的基礎上,構建“生物質能資源數據庫信息系統”的構想得以落地并煥發生機。該系統不再依賴傳統、粗放的經驗估算或周期漫長的人工普查,而是能夠實現:
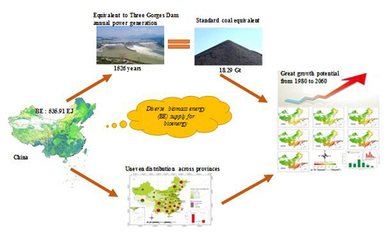
- 資源存量精準盤點:系統可以實時或定期估算特定區域內(從農田到區域尺度)可用作生物質能源的農作物殘余物(如秸稈、稻殼)、能源作物(如芒草、柳枝稷)的產量、分布及變化趨勢。結合作物生長模型與實時數據,預測其潛在生物質能蘊藏量變得前所未有的精確。
- 生長過程動態監控與品質評估:物聯網監測的不只是產量,更能追蹤影響生物質品質的關鍵參數。例如,對于能源作物,其纖維素、半纖維素、木質素的含量直接影響后續轉化效率。通過關聯生長環境數據與歷史品質數據,系統可對生物質原料的品質進行初步評估與分級,為高附加值利用提供依據。
- 收集、運輸與供應鏈優化:系統可整合地理信息、交通路網、天氣預測等數據,結合實時獲取的生物質資源分布熱圖,智能規劃最優的收集路線、儲存點布局及運輸方案,大幅降低物流成本,提高整個供應鏈的響應速度與效率。
- 決策支持與可持續管理:數據庫信息系統能為政府、企業和農戶提供強大的決策支持。政府可據此制定更科學的生物質能產業規劃與補貼政策;能源企業可精準選址建設轉化工廠;農戶則能獲得何時何地以何種方式出售農業殘余物收益最大的建議。系統有助于監控生物質采集對土壤肥力、生態平衡的影響,確保資源開發的可持續性。
- 促進循環農業與碳資產管理:精確追蹤農作物殘余物的去向(是還田、飼料化、還是能源化),有助于完善農業碳足跡核算。將生物質能利用與碳減排效益掛鉤,該系統可成為未來農業領域參與碳交易、實現生態價值轉化的重要數據基石。
構建這一系統也面臨挑戰,包括農田物聯網設備部署與維護成本、海量異構數據的融合與標準化、數據安全與隱私保護、以及跨部門(農業、能源、環境、交通)的數據共享與協作機制等。
隨著5G、邊緣計算、人工智能等技術與物聯網的進一步融合,未來的生物質能資源數據庫信息系統將更加智能自主。它不僅能“感知”和“記錄”,更能“分析”與“預測”,甚至通過反饋控制灌溉、施肥等環節,主動“培育”出更符合能源轉化需求的生物質原料。
物聯網連接農作物,遠不止于提升種植效益。它正作為關鍵紐帶,將傳統的農業生產與現代的能源信息系統深度耦合,催生出一個數據驅動的生物質資源管理新時代。這不僅是技術的進步,更是向著資源高效、環境友好、能源可持續的未來農業與能源體系邁出的堅實一步。構建和完善這樣的系統,對于保障國家能源安全、推動鄉村振興、實現“雙碳”目標具有重大而深遠的戰略意義。